Sociedad -
Coronavirus
La EMA decidirá en octubre si autoriza administrar una tercera dosis de Pfizer
La agencia comenzó a principios de septiembre a evaluar la idoneidad de una dosis de recuerdo para todas las personas mayores de 16 años y emitirá su decisión el próximo mes de octubre.
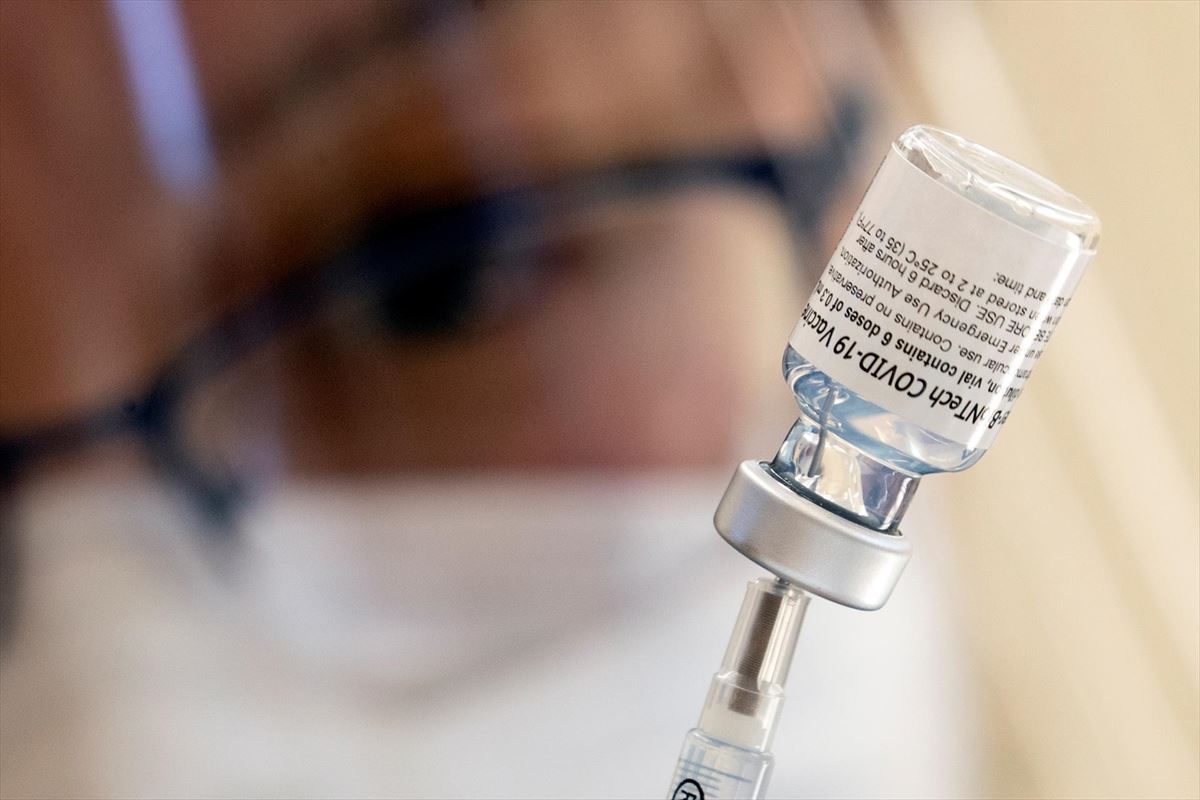
Agencias | EITB MEDIA
Euskaraz irakurri: Europako Sendagaien Agentziak urrian erabakiko du Pfizerren hirugarren dosia baimentzen duen
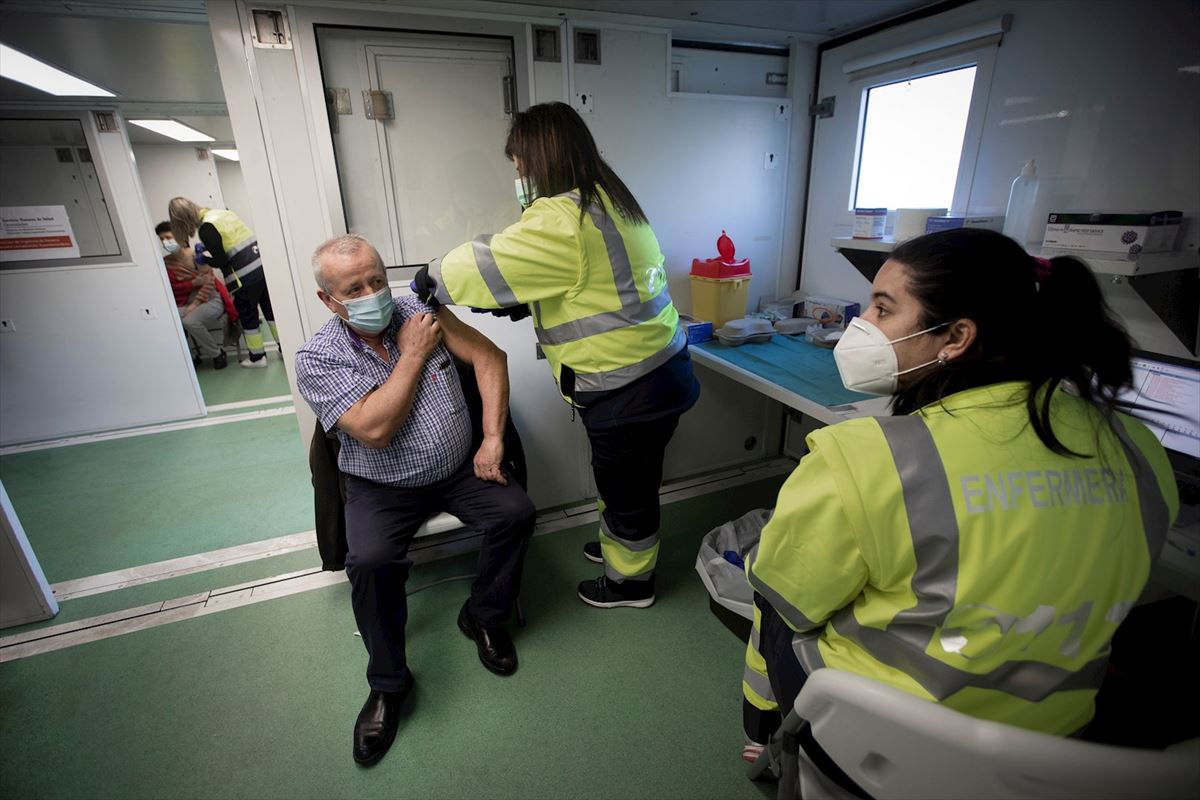
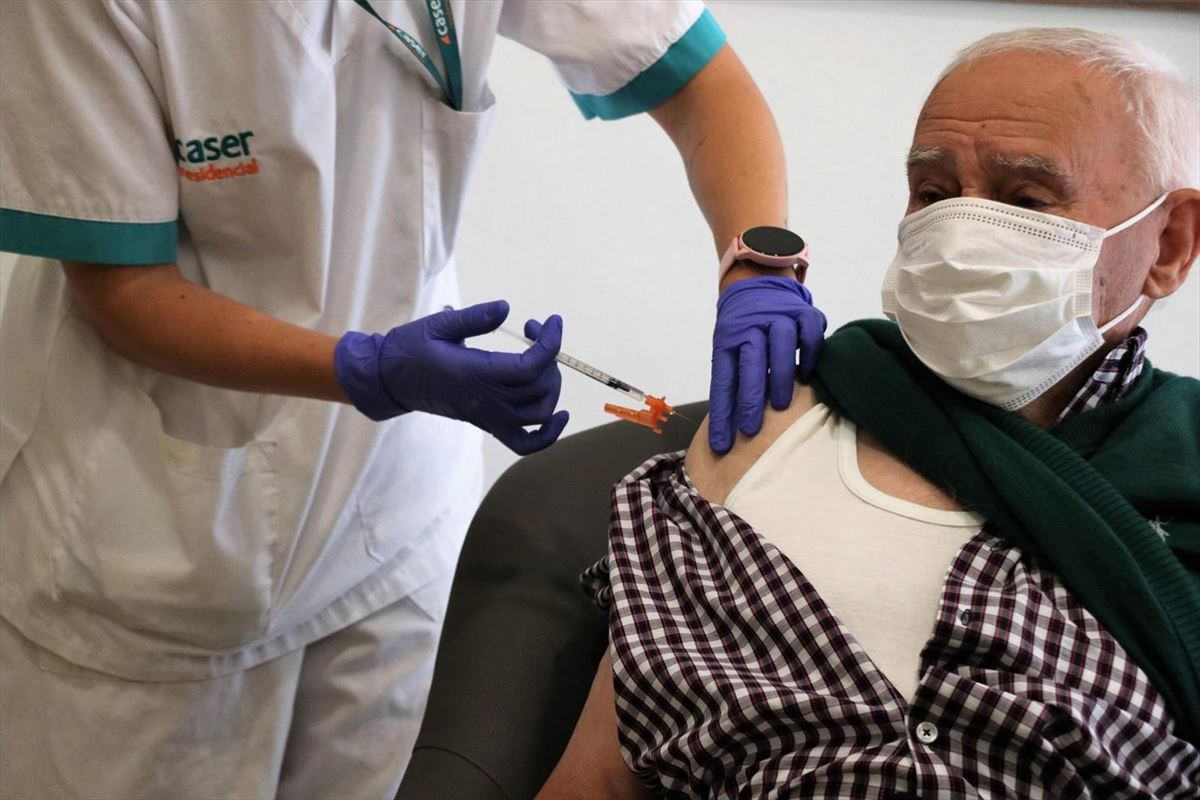
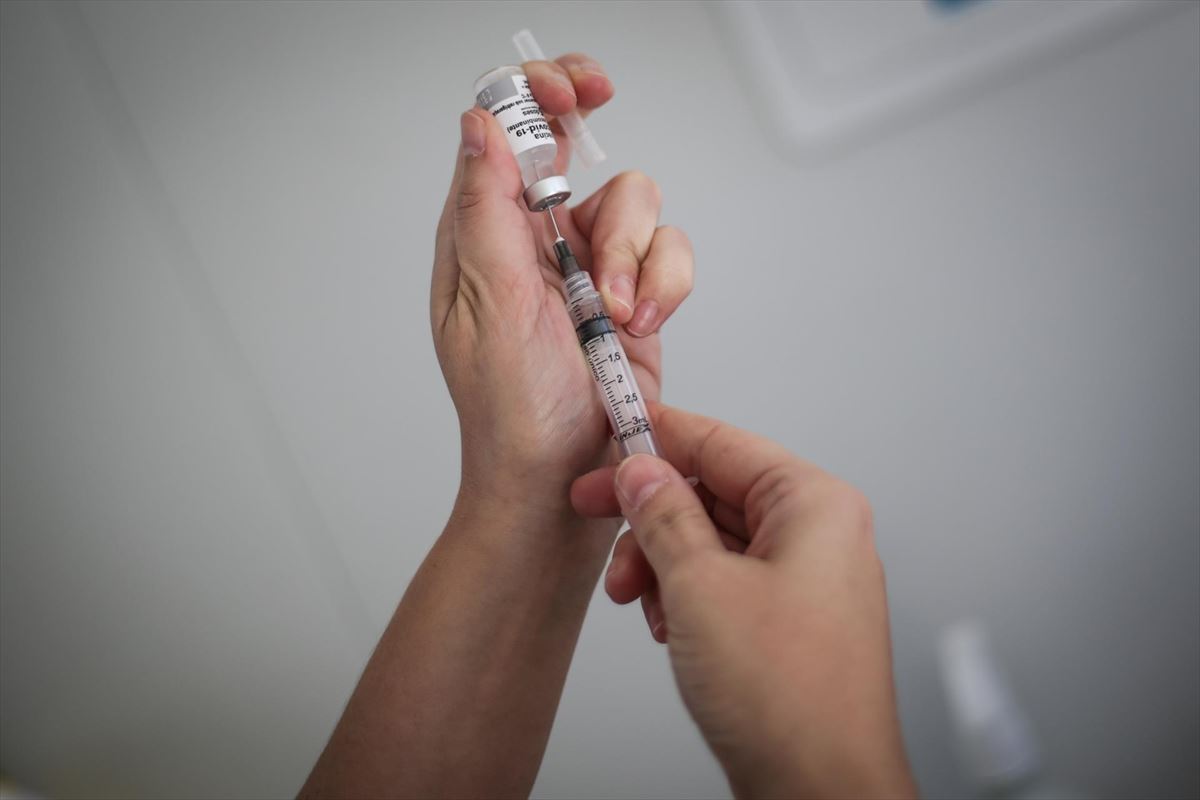
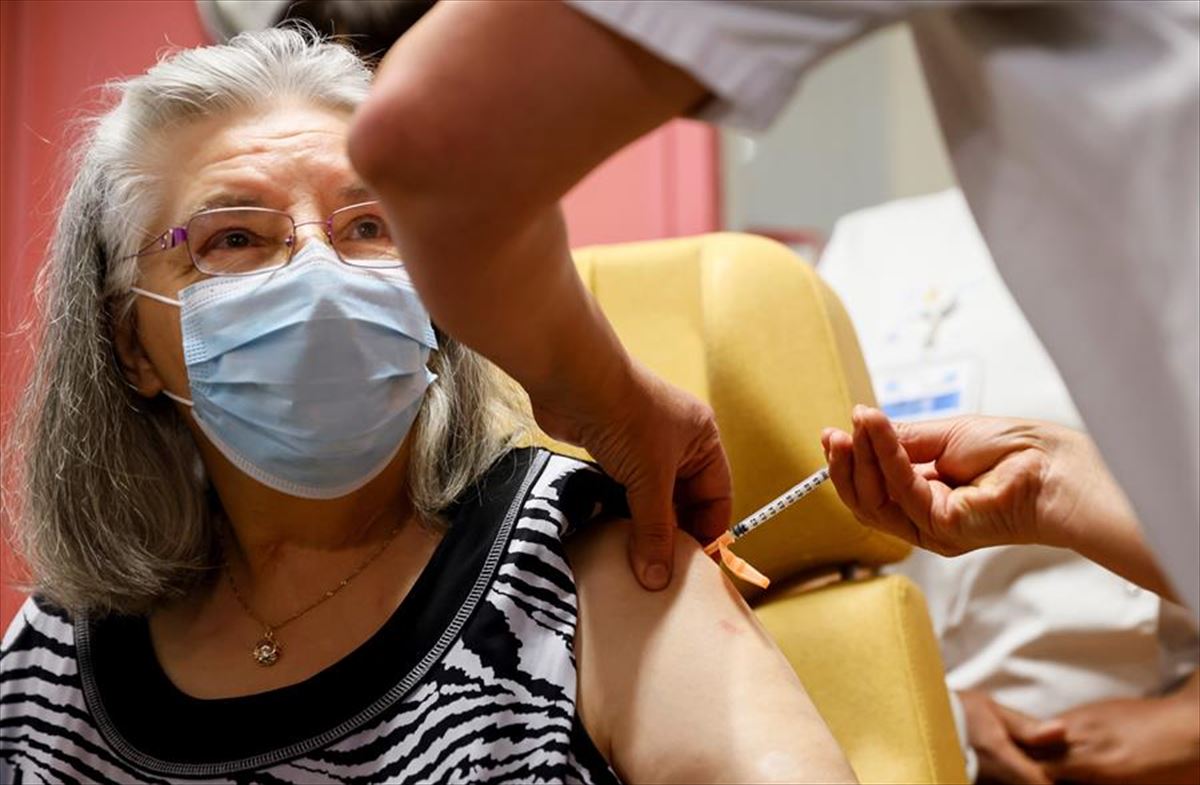
La Agencia Europea de Medicamentos (EMA) decidirá a principios de octubre si autoriza administrar una tercera dosis de la vacuna contra la covid-19 de Pfizer-BioNTech.
La EMA está "siguiendo rigurosamente el camino" de "no apresurarse en dar dosis de refuerzo si no hay una indicación clara de que sean necesarias" y para el regulador europeo es "importante" basar siempre su decisión en "evidencias científicas y no en ninguna presión", ha advertido Marco Cavaleri, jefe de Estrategia de Vacunas de la EMA.
La evidencia actual, dice, es "cada vez más clara sobre la necesidad de considerar" una dosis adicional para las personas que desarrollen una respuesta insuficiente a las vacunas de la covid-19, como los inmunodeprimidos, una inyección que formaría "parte de su vacunación primaria" contra el coronavirus, lo que no se califica de "dosis de refuerzo".
En una conferencia de prensa virtual, Cavaleri ha explicado que diferentes estudios señalan que las personas inmunodeprimidas "no siempre responden" a las vacunas de la covid-19 y que una tercera dosis de una vacuna de ARN mensajero un mes después de la segunda es "capaz incrementar la respuesta" y la protección contra la enfermedad causada por el SARS-CoV-2.
Los datos de estos estudios se encuentran ya en manos del comité de medicamentos humanos (CHMP), que espera concluir "a principios de octubre" su evaluación ya hacer una recomendación oficial a los Estados miembros, aunque muchos países están ya ofreciendo una dosis adicional a grupos vulnerable, sin esperar a la decisión de la EMA.
La agencia comenzó a principios de septiembre a evaluar la idoneidad de una dosis de recuerdo, seis meses después de la segunda, para las personas mayores de 16 años. La EMA, que depende de la Comisión Europea, ya apuntó entonces que la evidencia era más clara sobre la necesidad de considerar dosis adicionales" a pacientes inmunodeprimidos.
Pfizer-BioNTech aboga por una tercera inyección generalizada porque asegura que la eficacia de la vacuna se diluye con el tiempo. Así, presentó en septiembre los ensayos clínicos que avalan esta opción. La farmaceútica ha declinado hacer valoraciones sobre el anuncio de la EMA.